Šių metų pradžioje Filadelfijos ir Peno vaikų ligoninės mokslininkai sukūrė pirmąjį tokio tipo vaistą, pritaikytą unikaliai genetinei mutacijai, kad išgelbėtų kūdikį, vardu Baby KJ, nuo mirties nuo reto kepenų sutrikimo.
KJ Muldoono gydytojai naudojo CRISPR – šurmuliuojantį mokslinio įrankio, veikiančio kaip „rasti ir pakeisti“ komanda, santrauką, kad nustatytų genetinę rašybos klaidą, dėl kurios jo kūnas negalėjo gaminti pagrindinio fermento, skaidančio baltymus. Tada jie suleido vaistą su genetinio kodo dalelėmis, kad ištaisytų rašybos klaidą ir žymiai pagerintų jo galimybes išgyventi.
Vaistas niekada nebus skiriamas kitam pacientui, tačiau mokslininkai mano, kad šis metodas gali būti atkartotas siekiant padėti kitiems pacientams, sergantiems retomis ligomis, pritaikant pagal užsakymą pagamintus vaistus, kad būtų nukreiptos skirtingos genetinės rašybos klaidos.
Dabar jie turi galimybę išbandyti savo teoriją. Lapkričio 12 d. JAV maisto ir vaistų administracija paskelbė apie naują požiūrį į klinikinius tyrimus, skirtus išbandyti unikalius vaistus, tokius kaip CHOP ir Penn gydytojai sukūrė KJ.
Šis metodas sukuria kelią į reguliavimo patvirtinimą ir draudimo apsaugą retų ligų gydymui, kuris praeityje turėjo mažai galimybių patekti į rinką, nes yra naudingas tiek mažai žmonių.
FDA protokolas sprendžia ilgalaikį iššūkį kuriant retų ligų gydymo būdus: mokslininkai stengiasi identifikuoti pakankamai pacientų, kad bandymų metu būtų sukurta kritinė masė, o farmacijos įmonės nenori išleisti milijonų dolerių ir metų, kad sukurtų vaistą, kuris galiausiai bus naudingas labai nedaugeliui žmonių.
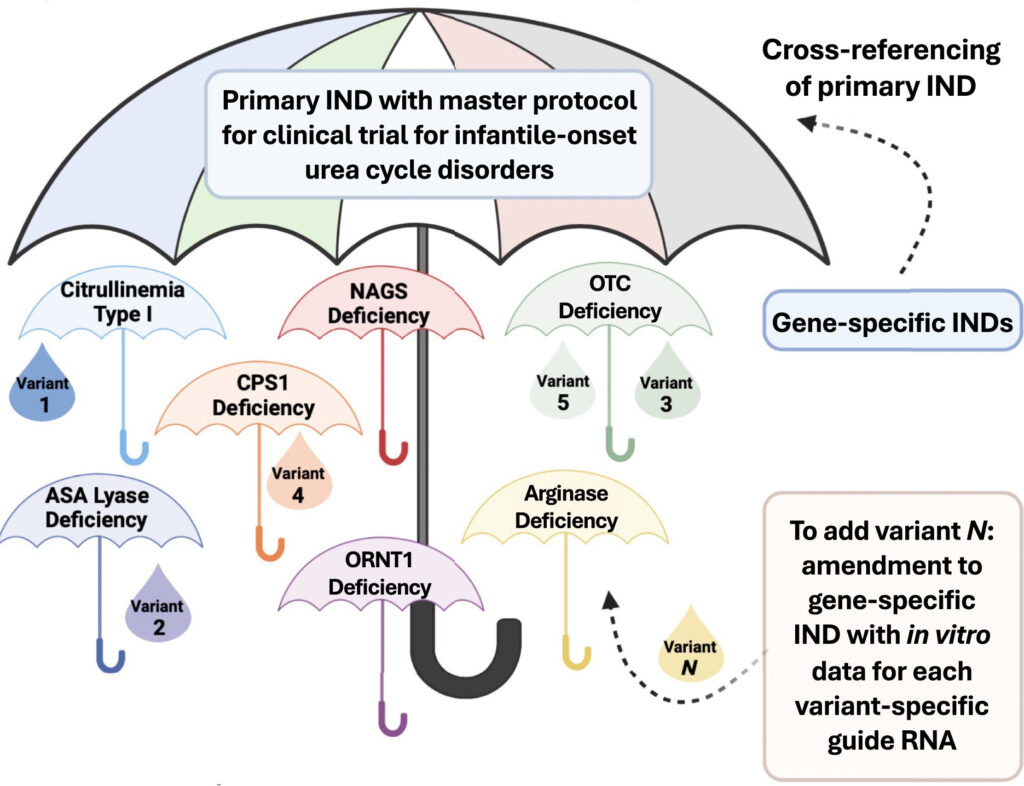
Dabar FDA naujasis „tikėtino mechanizmo“ protokolas sukurs būdą Filadelfijos tyrėjams išbandyti CRISPR sistemą, skirtą gydyti pritaikytą genų terapiją karbamido ciklo sutrikimams, susijusiems su bet kuriuo iš septynių genų. Mechanizmas išliks toks pat, bet kiekvienam pacientui skiriama injekcija bus pritaikyta pagal unikalią genetinę mutaciją.
Filadelfijos komanda, kuriai vadovauja kardiologas ir pirmaujantis Pensilvanijos universiteto genų redagavimo ekspertas Kiranas Musunuru ir Filadelfijos vaikų ligoninės medžiagų apykaitos ligų specialistė Rebecca Ahrens-Nicklas, tikisi, kad jų darbas bus retų ligų vaistų kūrimo pavyzdys.
„Kaip akademikai, laikome save ieties viršūne, einame ten, kur įmonės nenori eiti“, – sakė Musunuru.
Pasak jo, jų tikslas yra parodyti farmacijos įmonėms, kad retų ligų vaistų kūrimas yra įmanomas didesniu mastu. Jie paskelbė išsamią informaciją apie savo sąveiką su FDA Amerikos žmogaus genetikos žurnalas.
Nors kiekviena reta liga yra nedažna, milijonai žmonių serga reta liga. Daugelis jų turi bendrų savybių, kurias galima išspręsti naudojant pritaikomą vaistą.
CRISPR naudojimas retoms ligoms gydyti
KJ gydymas buvo nauja CRISPR, genų redagavimo įrankio, kurio kilmė mažai tikėtina, programa, apimanti jogurto gamyboje naudojamų bakterijų kokybės kontrolės testus.
Mokslininkai išsiaiškino, kad bakterijos saugo jas atakuojančių virusų DNR. Šie mikrobų „puodelio kadrai“ gali būti naudojami siekiant tiksliai nustatyti genetinę rašybos klaidą paciento DNR.
Tada tam tikros rūšies fermentas naudojamas rašybos klaidai „iškirpti“ ir ją ištaisyti arba pašalinti.
Anksčiau šiais metais KJ gydytojai paskelbė, kad jie panaudojo technologiją kurdami individualų vaistą, naudodami informaciją apie jo specifinę genų mutaciją.
Jie dirbo su išorės tyrimų ir gamybos partneriais, kad greitai pagamintų vaistą ir išbandytų jo saugumą. Jiems buvo suteiktas greitas FDA leidimas pagal taisykles, skirtas paspartinti retų ligų gydymą.
Šis požiūris buvo išgelbėtas KJ, kuris birželio mėnesį grįžo namo po 307 dienų ligoninėje ir jam reikės nuolatinio gydymo.
Identiškas vaistas niekada negali būti naudojamas kitam pacientui. Ir rankomis gaminti vaistus retomis ligomis sergantiems pacientams po vieną neįmanoma.
Remiantis KJ gydymu
Kad pasiektų daugiau pacientų, kuriems taikoma genų redagavimo terapija, Musunuru ir Ahrens-Nicklas turėjo rasti būdą, kaip sukurti vaistą, kuris galėtų būti gaminamas didesniu mastu.
Be to, jie turėjo turėti galimybę kreiptis dėl FDA patvirtinimo – auksinio JAV vaistų saugos standarto, be kurio dauguma draudimo kompanijų neapdraus vaistų.
Paprastai vaistų kūrėjai daugiausia dėmesio skiria tam tikram konkrečios ligos gydymui, investuodami milijonus dolerių iki dešimties metų, kad vaistas būtų pateiktas rinkai.
Vietoj to, Musunuru ir Ahrens-Nicklas dirbo su FDA, kad sukurtų bandymo protokolą, kuris leistų jiems išbandyti vaistų platformą, kurią būtų galima pritaikyti individualiems pacientams.
„Galingumas skaičiais yra tikras dalykas, kad būtų galima pasakyti, ar vaistas yra veiksmingas“, – sakė Musunuru. „Jei bandytumėte stoti prieš kiekvieną iš šių septynių, tai kainuotų pernelyg brangiai.
Jie planuoja išlaikyti tokius pačius pagrindinius gydymo elementus: CRISPR nustatys genetinę rašybos klaidą, o pacientai gaus vaistą su DNR dalimis, kad ją ištaisytų. Tikslus genas, į kurį bus nukreipta, priklausys nuo kiekvieno paciento specifinio sutrikimo.
Jie planuoja išbandyti vaistą pacientams, turintiems karbamido sutrikimų, kurie turi įtakos organizmo gebėjimui skaidyti baltymus ir išskirti amoniaką, nes šios būklės turi daugiau matomų „biožymenų“ arba rodiklių, rodančių, kokia yra problema ir ar genų redagavimo terapija padėjo.
„Mes matuojame, kas kaupiasi ir ko mums trūksta”, – sakė Ahrens-Nicklas.
Pavyzdžiui, KJ turėjo genetinę mutaciją, kuri neleido jo kūnui sukurti baltymus apdorojančio fermento. Gydytojai galėjo lengvai patikrinti, ar jo organizme trūksta reikiamo fermento ir ar jo organai negauna baltymų.
Suteikę jam pagal užsakymą pagamintą gydymą, jie pamatė, kad fermentų skaičius padidėjo ir kad buvo apdorojama daugiau baltymų.
Naujas FDA retų ligų gydymo būdas
A Naujosios Anglijos medicinos žurnalas Straipsnyje, kuriame aprašomas jų planas, FDA komisaras Marty Makary ir Vinay Prasad, agentūros vyriausiasis medicinos ir mokslo pareigūnas, nurodė KJ vieno paciento genų terapiją kaip pavyzdį, kaip jie tikisi, kad naujasis protokolas padės pasiekti daugiau pacientų.
KJ terapiją iš pradžių patvirtino FDA, atlikdama pagreitintą vienos savaitės peržiūros procesą, skirtą vienam pacientui, paprastai sunkiai sergančiam itin reta liga.
Prasadas ir Makary rašė, kad „dabartinės taisyklės yra sudėtingos ir be reikalo reikalaujančios, užtikrina neaiškią pacientų apsaugą ir slopina naujoves“.
Jie rašė, kad KJ atvejis „išryškina galimybę“ vienam pacientui skirti terapiją sukurti vaistą, kurį būtų galima modifikuoti, kad būtų galima gydyti kitas panašias retas ligas.
„Praėjus beveik 30 metų po žmogaus genomo sekos nustatymo, pagal užsakymą pritaikytos terapijos yra artimos tikrovei“, – rašė jie.
2025 m. „The Philadelphia Inquirer, LLC“. Platina Tribune Content Agency, LLC.