Stemplės adenokarcinoma (EAC), viena iš dviejų pagrindinių stemplės vėžio formų, yra šeštasis mirtiniausias vėžys visame pasaulyje, kuriam nėra veiksmingos tikslinės terapijos. Pacientai turi pasikliauti chemoterapija kaip priežiūros standartu, kuris pradedamas prieš chirurgines intervencijas kaip vadinamąją „neoadjuvantinę chemoterapiją“ (NACT), tikintis susitraukti ar kontroliuoti navikus. Tačiau dauguma pacientų tampa atsparūs tam tikriems NACT, dėl kurių atsiranda prasta rezultatai.
Atsižvelgiant į tai, kad trūksta terapinių alternatyvų, ir atsakytojai, ir neatsakantys asmenys ir toliau gauna vieną iš turimų chemoterapijų, nežinodami, ar tai veiks. Net ir reaguojant, pasirinkta chemoterapija gali nevisiškai sustabdyti jų navikų progresą ir metastazavimą, ir ji gali turėti toksišką šalutinį poveikį organizmui. Kritinis nepatenkintas poreikis yra suasmenintas, paciento specifinio tikslumo onkologijos modelis, kuris gali tiksliai numatyti paciento reakciją į skirtingus NACT.
Tyrėjai iš biopsuotų EAC ląstelių išaugino vadinamuosius „organoidus“, tai yra 3D stemplės miniorgans, susidarę su audiniais specifinėmis kamieninėmis ląstelėmis, pasižyminčiomis stemplės epitelio gleivinės kritinėmis savybėmis. Tačiau jiems trūksta svarbių paciento specifinio naviko mikroaplinkos (TME) komponentų, tokių kaip stromos fibroblastai ir kolageno skaidulos, todėl jie nerodo tokių pačių atsakymų į NACT kaip ir tikrieji navikai.
Dabar tyrimų bendradarbiavimas, kuriam vadovauja Ph.D. Donaldas Ingberis, MD įkūrėjas Wyss biologiškai įkvėptos inžinerijos inžinerijos inžinerijos direktorius Harvardo universitete ir Lorenzo Ferri, MD, kuris vadovauja krūtinės ląstos ir viršutinės virškinimo trakto skyriui Montreale Montrealyje.
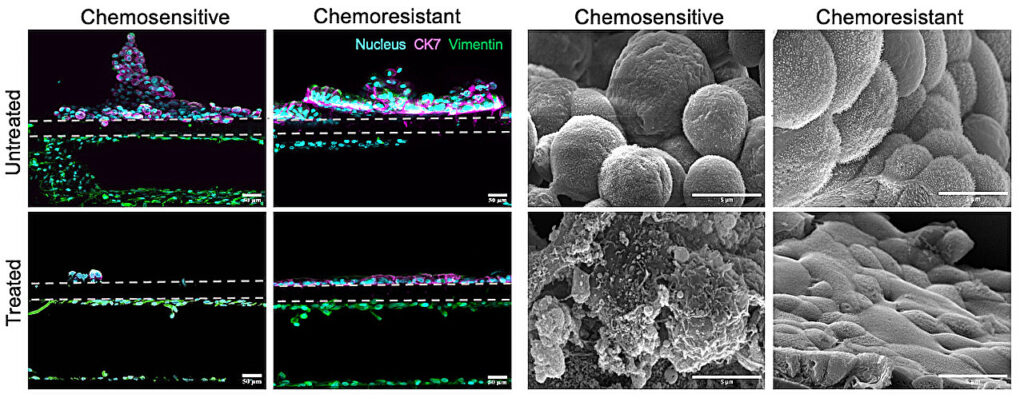
Tyrėjai pasitelkė Wyss instituto žmogaus organų mikrofluidinės kultūros technologiją ir panaudojo ją kultūrai EAC organoidams šalia stromos ląstelių, išskirtų iš tų pačių biopsijų, kurias „McGill“ komanda gavo iš EAC pacientų klinikinės kohortos tyrime, kad būtų sukurtos konkrečios pacientams būdingi, TMEVIZINIAI VYNINIŲ CHIP modeliai. Sužinojusi kai kuriuos būdingus TME sudėtingumą in vitro, komanda sugebėjo numatyti pacientų naviko reakcijas į standartinį NACT daug tiksliau nei statiškesni, mažiau sudėtingi 3D organoidų modeliai.
Kadangi požiūris gali duoti rezultatus per 12 dienų nuo modelio pradžios, tai leidžia greitai stratifikuoti EAC pacientus į reaguojančius asmenis ir neatsakančius asmenis, ir ištirti nestandartinius NACT, pagrįstus skirtingais chemoterapijos agentais atspariems pacientams kliniškai naudingu laikotarpiu. Rezultatai pateikiami Transliacinės medicinos žurnalas.
„Šis į pacientą orientuotas požiūris stipriai remiasi mūsų ankstesnėmis sėkme, naudojant žmogaus organų lustų technologiją, kad būtų galima pakartoti kiekvieno atskiro vėžio paciento TME už jų kūno ribų, kad galėtume nustatyti vaistų derinį, kuris geriausiai veiks tam labai pacientui. Šis naujas būdas, susijęs su personalizuotu vaistu, gali būti įgyvendintas klinikiniuose centruose, kuriuose daugiausia dėmesio skiriama pacientams, kuriems kenčia nuo daugelio skirtingų vėžio rūšių, pavyzdžiui, mūsų kolektorių, kuriems buvo atlikta pacientams, kurie turi esminius vėžį, priežiūrą.
„Galbūt ne mažiau svarbu, kad jis taip pat gali būti naudojamas kaip ikiklinikinis bandymas, siekiant sugriauti naują pagrindą kuriant naviko ar stromos gydymą vėžiu sergantiems pacientams ir sudaryti sąlygas atrasti biomarkerius, kurie galėtų būti naudojami stebėti ir optimizuoti vaistų poveikį šiems pacientams.”
Ingber taip pat yra Judo folkmanas Harvardo medicinos mokyklos ir Bostono vaikų ligoninės kraujagyslių biologijos profesorius bei Hansjörg Wyss biologiškai įkvėptos inžinerijos profesorius Harvardo Johno A. Paulsono inžinerijos ir taikomųjų mokslų mokykloje.
Stemplės patologijų modeliavimas
„Ingber“ ir „Ferri“ komandos pradėjo bendradarbiauti jau 2023 m., Atlikdami ankstesnį tyrimą, kuriame jie modeliavo Barrett stemplę mikrofluidinių organų luste. Barrett stemplė gali būti piktybinis EAC pirmtakas, kuris, kaip manoma, yra patologinių pokyčių serijos, kurią išgyvena apatinio stemplės epitelio gleivinė.
Tai prasideda nuo uždegimo, kurį dažniausiai sukelia rūgšties refliuksas, ir tęsiasi per stemplės audinį transformuojant į hiperproliferuojantį skrandį ir plonųjų žarnas panašų audinį (Barrett'o stemplę), kad galų gale sukeltų šias labai dauginančias nenormalias ląsteles į vėžio ląsteles.
Svarbu tai, kad šiuos piktybinius pokyčius lemia ne tik molekuliniai ir ląsteliniai procesai stemplės epitelio gleivinėje, bet ir jo pagrindinėje „stroma“, kurią sudaro fibroblastų ląstelės, kurios bendrauja su vėžio ląstelėmis per nuolatinį molekulių mainus, taip pat yra imuninių ląstelių ir kraujagyslių.
„Kadangi ankstesniame mūsų darbe mes ištikimai pakartojome ankstesnius patologinio proceso etapus, galinčius sukelti EAC, būtent Barrett stemplę, mūsų naujajame tyrime mes greitai pertvarkėme į jo vėžinį rezultatą“,-abiejų tyrimų metu sakė antrasis autorius Elee Shimshoni.
„Tik atkurdami pagrindinius TME komponentus ir imituodami kai kuriuos jo skysčių srautus, kuriuos paprastai teikia skysčiai, esantys aplinkinėse ląstelėse (intersticinis skystis) ir palaikydami kraujagysles, mes sugebėjome pasiekti fiziologiškai reikšmingą vaistų poveikį, ir tiksliai numatėme, kad pacientams specifiškos reakcijos į asmeninius EAC CHITS nebuvo.”
Nuo pacientų iki vėžio traškučių ir atgal
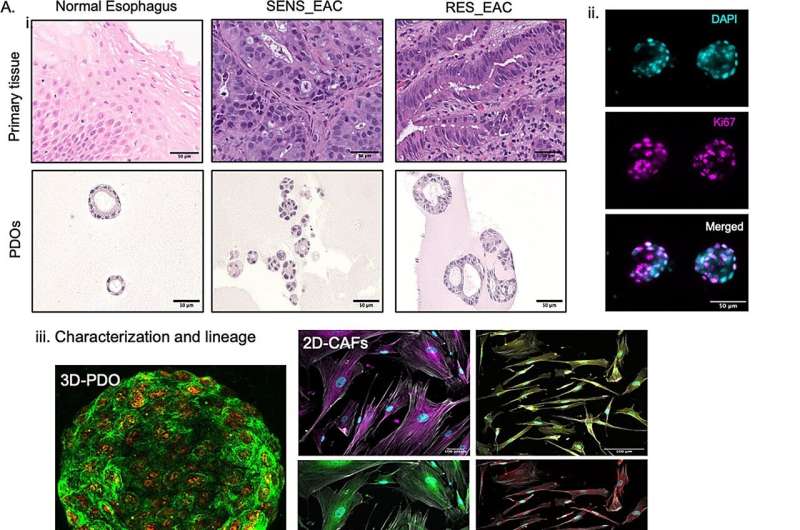
Komanda sukūrė savo TME imituojantį EAC mikroschemą, pirmiausia generuodama suasmenintus EAC organoidus iš biopsijų, kurias jie endoskopiškai gauna iš pacientų, kuriems naujai buvo diagnozuota EAC, tačiau dar nebuvo gydomi. Pirmasis autorius Sanjima Pal, Ph.D. ir kiti „McGill University“ sveikatos priežiūros centro „Ferri“ komandos nariai, kur FERRI gydo pacientus, sergančius stemplės vėžiu, įvaldė galimybę sukurti didelę nuoseklumą pacientams suderintus stemplės organoidus.
Tada komanda pašalino organoidus iš kultūros patiekalo, suskaidė juos į savo sudedamąsias ląsteles, augino ląsteles viename iš dviejų lygiagrečių mikrofluidinės lusto kanalų, kurių dydis yra atminties lazda, ir pridėjo su naviku susijusius fibroblastus iš tų pačių pacientų prie kito kanalo, kad sudarytų gretimi naviko stromą.
Abu kanalai yra atskirti porėta membrana, leidžianti vėžio ir stromos audiniams laisvai keistis molekulėmis, kaip tai darytų realiame navike. Galiausiai tyrėjai į docetakselio pagrindu pagamintą tripleto chemoterapijos kokteilį į maistines skysčius, tekančius per stromos kanalą, naudojant vaistų koncentraciją ir ekspozicijos laiką, kuris atkartoja chemoterapijos ciklą EAC sergantiems pacientams.
Aštuonių pacientų grupėje visi EAC lustai tiksliai numatė savo atsakymus į NACT per 12 dienų. Keturiuose iš žetonų chemoterapija privertė EAC ląsteles mirti, o kitose keturiose žetonuose EAC ląstelės išgyveno chemoterapiją. Šie rezultatai puikiai koreliavo su pacientų reakcija į tą pačią chemoterapiją ir jų išgyvenamumą po chirurginės EAC navikų rezekcijos.
Kiti tyrimo autoriai buvo Salvador Flores Torres, Mingyang Kong, Kulsum Tai, Veena Sangwan, Nicholas Bertos, Swneke Donovan Bailey ir Julie Bérubé.