Mokslininkai sukūrė naują junginį, kuris galėtų pasiūlyti proveržį pasaulinėje kovoje su tuberkulioze, mirtingiausia istorijos infekcine liga.
Neseniai paskelbtas tyrimas Prigimtis Aprašomas naujojo junginio, žinomo kaip CMX410, gydymo potencialas. Vaistas vienareikšmiškai nukreiptas į esminį fermentą Mycobacterium tuberculosis – bakterijai, atsakingai už tuberkuliozę. Svarbu tai, kad šis junginys netgi pasirodė veiksmingas nuo vaistams atsparių infekcijų, kurios yra paplitusios visame pasaulyje ir kelia didelį iššūkį kontroliuoti ligos plitimą ir progresavimą.
Tyrimui vadovavo Ph.D. James Sacchettini, Rodgerio J. Wolfe-Welcho fondo fondo pirmininkas Science, Teksaso A&M žemės ūkio tyrimų mokslininkė ir Teksaso A&M Žemės ūkio ir gyvybės mokslų kolegijos Biochemijos ir biofizikos departamento bei Biofizikos departamento bei Biofizikos katedros. Prie jo prisijungė Case McNamara, Ph.D., vyresnysis infekcinių ligų direktorius Calibr-Skaggs inovatyvių vaistų institute, Scripps tyrimų, skirtų ne pelno siekiančiam vaistų plėtros skyriui, skirtą pagreitinti naujos kartos vaistus.
„Daugelis žmonių galvoja apie tuberkuliozę kaip praeities ligą“, – teigė Sacchettini. „Tačiau iš tikrųjų tai išlieka pagrindine visuomenės sveikatos problema, reikalaujanti didelio dėmesio, bendradarbiavimo ir naujovių, kad būtų įveikti.”
Protingesnis būdas kovoti atgal
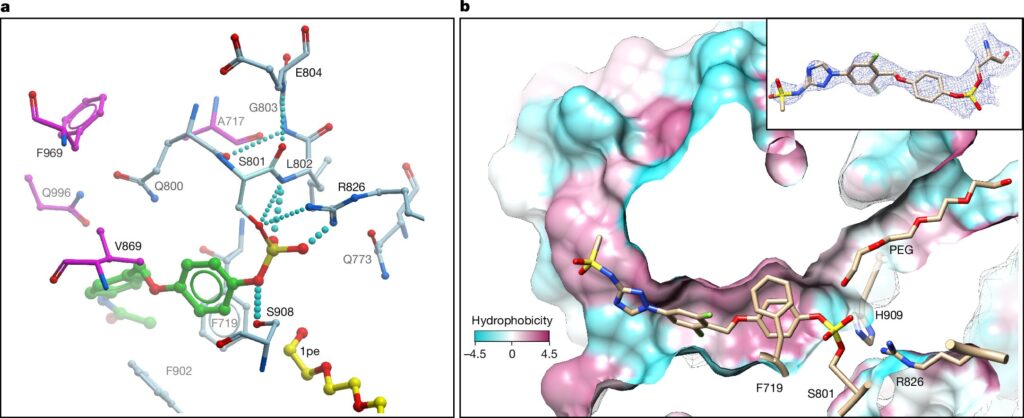
Naujasis junginys, identifikuotas atliekant „AgriLife Research“ ir „Calibr-Skaggs“, veikia blokuodamas esminį fermentą, poliketido sintazę 13 arba PKS13, kad M. tuberculosis turi sukurti savo apsauginę ląstelių sienelę. Be šio baltymo funkcionalumo bakterijos negali išgyventi, kad sukeltų infekciją.
Daugiau nei dešimtmetį mokslininkai pripažino šį baltymą kaip didelės vertės taikinį kovojant su tuberkulioze. Nepaisant savo galimybių, vaistų kūrimo pastangos ne kartą netrukdė – daugiausia dėl to, kad junginiai turi išvalyti aukštą juostą tiek saugumui, tiek terapiniam rezultatams.
Unikalus „CMX410“ mechanizmas daro jį labai konkrečiu savo tikslui, kuris reiškia palankų saugos profilį. Įtraukdami reaktyvią cheminę grupę, kuri sudaro negrįžtamą ryšį su kritine PKS13 vieta, tyrėjai sustiprino junginio selektyvumą, sumažindami potencialiai neigiamą ne tikslinio poveikį. Ši modifikacija taip pat sumažina atsirandančio pasipriešinimo tikimybę.
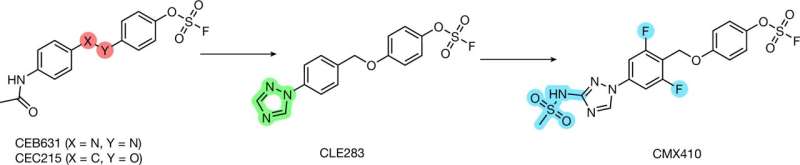
Pridedant šią pagrindinę cheminę grupę, buvo atlikta naudojant „Click Chemistry“ – metodą, kuris užfiksuoja molekules kartu kaip dėlionės gabalėlius. „Click Chemistry“ sukūrė bendraautorius Barry Sharpless, Ph.D., WM Keck chemijos profesorius Scripps Research ir du kartus Nobelio laureatas, ir tai paskatino sukurti plačias cheminių junginių bibliotekas.
„Ši technika yra naujas vaistų projektavimo įrankis“, – sakė A. McNamara. „Mes tikimės, kad ateinančiais metais bus išplėsta jo panaudojimas, kad padėtų išspręsti visuomenės sveikatos problemas, turinčias kritinio poreikio, įskaitant tuberkuliozę.”
Ankstyvieji rezultatai pasirodo saugūs ir veiksmingi
Komanda pradėjo tirti junginių, kuriais dalijasi „Sharpless“ laboratorija, biblioteką, kad nustatytų molekules, kurios galėtų slopinti M. tuberculosis bakterijų augimą.
Po intensyvaus optimizavimo, siekiant pagerinti sudėtinių potencialą ir kitas farmakologines savybes, kurioms vadovauja „Calibr-Skaggs“ tuberkuliozės komandos nariai ir pirmieji autoriai Baiyuan Yang, Ph.D., Medicinos chemijos asocijuotasis direktorius, ir Paridhi Sukheja, Ph.D., tyrėjas, CMX410, CMX410.
Yang, kuris vadovavo chemijos optimizavimui, teigė, kad komanda ištyrė daugiau nei 300 analogų, kad nustatytų junginį su tinkamu potencijos, selektyvumo ir saugos balansu. Galiausiai komanda ištyrė CMX410 prieš 66 M. tuberculosis padermes ir nustatė, kad ji veikia tiek laboratorijai, tiek daugialypiams vaistams atsparių padermių, surinktų iš realių pacientų.
„Nustatyti šį naują tikslą buvo įdomus momentas“, – sakė Sukheja, kuris vedė daugybę ankstyvųjų tyrimų, rodančių, kad CMX410 gali būti nukreiptas į anksčiau neištirtą geną. „Tai atvėrė visiškai naują kelią į priekį, ypač prieš padermes, kurios išmoko išvengti esamų gydymo būdų.”
Kituose ankstyvuose eksperimentuose tyrėjai nustatė, kad CMX410 gali būti saugiai derinamas su kitais tuberkuliozės antibiotikais. Tai buvo ypač svarbus šios ligos veiksnys, nes gydymo schemoms reikia kelių vaistų, kurie kartu ištisus mėnesius turi būti vartojami kartu.
Tyrėjai pradiniuose bandymuose gyvūnų modeliuose nerado neigiamo poveikio net ir esant maksimaliam dozės lygiui. Ir kadangi CMX410 yra labai būdingas jo tiksliniam baltymui, jie mano, kad tai mažai tikėtina, kad sutrikdys kitas naudingas bakterijas arba sukelia platesnį mikrobiomo disbalansą – įprastą įprastų antibiotikų šalutinį poveikį.
Pažanga link geresnio gydymo
Pridėjus specializuotą cheminę grupę, leidžiančią CMX410 negrįžtamai prisijungti prie savo taikinio, junginys tampa ypač selektyvus. Tokio tipo inhibitoriai išlieka jaudinančia ir nepakankamai išaiškinama vaistų klasė, todėl reikia atlikti papildomus tyrimus, kad būtų patvirtintas jų saugumas žmonėms.
Nepaisant to, tikslumas, unikalus mechanizmas, geras saugos profilis ir kitos pagrindinės savybės CMX410 tampa perspektyviu kandidatu į tuberkuliozę.
„Šie ankstyvieji rezultatai labai džiugina“,-teigė INNA Krieger, Ph.D., vyresnysis Sacchettini laboratorijos mokslininkė ir pirmoji tyrimo autorius. „Ląstelių sienomis nukreipiantys antibiotikai jau seniai buvo kertinis gydymo tuberkulioze akmuo. Tačiau po dešimtmečių plačiai paplitusio jų veiksmingumas mažėja dėl vaistams atsparių padermių.
„Mes stengiamės atrasti naujus vaistus, kurie sutrikdo esminius biologinius procesus ir nustato optimalius derinius su esamais vaistais, kad būtų galima sutrumpinti, saugesnius ir veiksmingesnius gydymo režimus. Per šias pastangas mes tikimės padėti pasauliui priartėti prie ateities be tuberkuliozės.”