Atlikdami atradimą, kuris galėtų paskatinti naujos kartos antidepresantų ir antipsichozinių vaistų vystymąsi, Sinajaus kalno ICAHN medicinos mokyklos tyrėjai sukūrė naujas įžvalgas apie tai, kaip kritinis smegenų receptorius veikia molekuliniu lygiu ir kodėl tai svarbu psichinės sveikatos gydymui.
Tyrimas, paskelbtas internetiniame numeryje Mokslo pažangadėmesys sutelkiamas į 5-HT1A serotonino receptorius, pagrindinį žaidėją, reguliuojantį nuotaiką, ir įprastą tradicinių antidepresantų ir naujesnių gydymo būdų, tokių kaip psichodelikai, taikinys. Straipsnis pavadintas „G baltymų potipio selektyvumo struktūriniais veiksniais serotonino receptoriuje 5-HT1A“.
Nepaisant klinikinės svarbos, šis receptorius išliko menkai suprantamas, nes daugelis jo molekulinių ir farmakologinių savybių iš esmės nepakankamai išnagrinėjo – kol dabar.
„Šis receptorius yra tarsi kontrolinė grupė, padedanti suvaldyti, kaip smegenų ląstelės reaguoja į serotoniną – pagrindinę cheminę medžiagą, susijusią su nuotaika, emocijomis ir pažinimu“, – sako Farmakologinių mokslų ir neuromokslų profesoriaus vyresnysis autorius Danielis Wackeris.
„Mūsų išvados paaiškina, kaip veikia ta valdymo pultas. Tai, kas ją keičia, yra, kaip ji patobulina signalus ir kur slypi jos ribos. Šis gilesnis supratimas galėtų padėti mums sukurti geresnes psichinės sveikatos būklės, tokios kaip depresija, nerimas ir šizofrenija, terapiją.”
Naudodama novatoriškus laboratorinius metodus, tyrimų komanda išsiaiškino, kad 5-HT1A receptoriai iš esmės yra sujungiami tam tikriems ląstelių signalizacijos keliams, palyginti su kitais-neatsižvelgiama į vaistą, naudojamą jam nukreipti.
Tačiau vaistai vis tiek gali paveikti stiprumą, su kuriuo suaktyvinti šie keliai. Pavyzdžiui, buvo nustatyta, kad antipsichozinis asenapinas (prekės pavadinimas Saphris) selektyviai naudojasi konkrečiu signalizacijos keliu dėl jo santykinai silpnos veiklos receptoriuje.
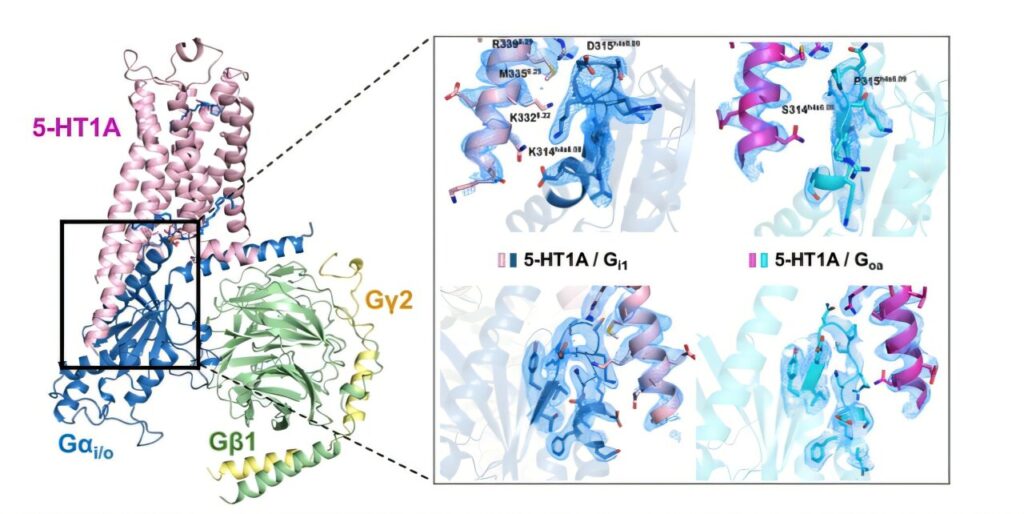
Norėdami išsamiau ištirti šiuos mechanizmus, tyrėjai sujungė eksperimentus su laboratorijoje užaugintose ląstelėse su didelės skiriamosios gebos krioelektronų mikroskopija-pažangiausia vaizdavimo technologija, atskleidžiančia molekulines struktūras beveik atominėje skiriamąja geba. Jų darbas buvo sutelktas į tai, kaip įvairūs vaistai suaktyvina 5-HT1A receptorius ir kaip receptorius sąveikauja su vidiniais signaliniais baltymais, vadinamais G baltymais.
Skirtingi signalizacijos keliai, kontroliuojami 5-HT1A receptorių, yra susieti su skirtingais nuotaikos, suvokimo ir net skausmo aspektais. Kadangi mokslininkai geriau supranta, kurie keliai yra suaktyvinti ir kaip, jie gali tiksliau suprojektuoti vaistus, kurie gydo specifinius simptomus ar sąlygas be nepageidaujamo šalutinio poveikio.
„Mūsų darbas pateikia molekulinį žemėlapį, kaip skirtingi narkotikų mygtukai“ ant šio receptoriaus – aktyvinantys ar nutildyti specifinius kelius, turinčius įtakos smegenų funkcijai “, – sako tyrimo pirmoji autorė Audrey L. Warren, Ph.D., buvęs Dr. Wackerio laboratorijos studentas, kuris dabar yra podoktorantūros tyrinėtojas Kolumbijos universitete.
„Supratę, kaip šie vaistai sąveikauja su receptoriais, galime pradėti numatyti, kurie požiūriai gali sukelti veiksmingesnį ar tikslinį gydymą, o kurie iš jų greičiausiai neveiks. Tai yra žingsnis kuriant naujos kartos terapiją, turint didesnį tikslumą ir mažiau šalutinio poveikio.”
Ypač stebinančioje išvadoje tyrėjai išsiaiškino, kad fosfolipidas-riebalų molekulės rūšis, randama ląstelių membranose-vaidina pagrindinį vaidmenį valdant receptoriaus aktyvumą, beveik kaip paslėptas bendras pilotas. Tai yra pirmas kartas, kai toks vaidmuo buvo pastebėtas tarp daugiau nei 700 žinomų tokio tipo receptorių žmogaus kūne.
Nors dabartiniams antidepresantams dirbti dažnai reikia savaičių, mokslininkai tikisi, kad šis naujas supratimas apie 5-HT1A signalizaciją galėtų padėti paaiškinti tuos vėlavimus ir sukelti greitesnį veikimo alternatyvas.
„Šis receptorius gali padėti paaiškinti, kodėl standartiniai antidepresantai užtrunka ilgai“, – sako dr. Wacker. „Supratę, kaip jis veikia molekuliniu lygmeniu, turime aiškesnį kelią kurti greitesnį, efektyvesnį gydymą ne tik dėl depresijos, bet ir dėl tokių sąlygų kaip psichozė ir lėtinis skausmas. Tai yra pagrindinis dėlionės dalis.”
Toliau tyrimų komanda planuoja įsigilinti į fosfolipidų „koeficiento“ vaidmenį ir išbandyti, kaip jų laboratorijoje pagrįstos išvados sulaiko sudėtingesniuose eksperimentuose. Jie taip pat siekia paversti šiuos atradimus realaus pasaulio junginiais, kurie galėtų tapti būsimiems psichiatriniams vaistams, remdamiesi ankstesne jų sėkme su narkotikų kandidatais, gautais iš psichodelinių vaistų.