Jeilio medicinos mokyklos (YSM) mokslininkai padarė pagrindinius laimėjimus, suprasdami, kaip gydyti fibrozines ligas, tokias kaip sklerodermija ir transplantato prieš šeimininką liga.
Fibrozinės ligos yra būklių, dažnai autoimuninių, grupė, kuriai būdingas per didelis audinių randėjimas. Jie gali smarkiai pakenkti pacientų gyvenimo kokybei, o kai kuriais atvejais gali kelti pavojų gyvybei – fibrozė sukelia maždaug 45 % visų mirčių išsivysčiusiose šalyse. Tačiau veiksmingų gydymo būdų nėra.
Dabar paskelbtame tyrime Kraujasmokslininkai sukūrė monokloninį antikūną, kuris yra perspektyvus kaip naujas gydymas pacientams. Ir a Gamtos komunikacijos Tyrimo metu ta pati komanda atrado signalizacijos kelią, kuris gali būti tarpininkaujantis fibrozei ir gali būti būsimos terapijos tikslas.
„Fibrozės gydymas yra nepaprastai nepatenkintas poreikis“, – sako Richard Flavell, Ph.D., YSM imunobiologijos profesorius ir vienas iš pagrindinių tyrimų tyrėjų. „Geresnis šių sąlygų supratimas greičiausiai suteiks naujų vaistų, kurie padės pacientams.”
Nauji terapiniai antikūnai sušvelnina fibrozę
Ankstesni tyrimai siejo baltymo, vadinamo epidermio augimo faktoriaus receptoriumi (EGFR), kuris padeda kontroliuoti ląstelių augimą ir dauginimąsi, reguliavimą su fibrozinėmis ligomis. Paprastai šis baltymas padeda skatinti žaizdų gijimą. Tačiau kai jis per daug suaktyvėja, gali susidaryti per didelis randų audinys, susijęs su fibroze.
2022 m. YSM mokslininkai nustatė, kad pacientų, sergančių sklerodermija – reta autoimunine liga, sukeliančia odos ir kartais vidaus organų fibrozę, odos mėginiuose padidėjo epiregulino – signalinės molekulės, kuri jungiasi su EGFR – lygis.
Jie iškėlė hipotezę, kad daugiau epiregulino gali sukelti pernelyg didelį EGFR aktyvavimą, o tai sukelia sklerodermijos fibrozę. Norėdami išbandyti šią idėją, jie naudojo antikūną, skirtą epiregulinui nukreipti ir sumažinti gyvūnų modeliuose, ir nustatė, kad jis pakeitė fibrozę.
Remdamasi šiomis išvadomis, savo naujausiame tyrime komanda sukūrė naują žmogaus antiepiregulino terapinį antikūną ir išbandė jo gebėjimą sušvelninti transplantato prieš šeimininką ligą, komplikaciją po kamieninių ląstelių arba kaulų čiulpų transplantacijos, kai donoro imuninės ląstelės atakuoja kūną ir kai kuriais atvejais sukelia fibrozę.
Pirma, mokslininkai palygino vienos ląstelės RNR sekos duomenis iš pacientų, sergančių sklerodermija ir transplantato prieš šeimininką liga, kad nustatytų bendrus mechanizmus, skatinančius abiejų ligų fibrozę, ir patvirtino, kad padidėjęs epiregulino reguliavimas yra dažna patologija.
„Iš tikrųjų išsiskyrė tai, kad epiregulino signalas, kaip anksčiau buvo pastebėtas sergant sklerodermija, buvo tikrai paryškintas pacientams, sergantiems šia fibrozine transplantato prieš šeimininką liga“, – sako Ianas Odell, MD, Ph.D., YSM dermatologijos docentas ir vienas iš pagrindinių tyrimų tyrėjų.
Tada komanda išbandė savo anti-EREG antikūnus humanizuotuose pelių modeliuose ir pacientų odos biopsijose ir nustatė, kad epiregulino slopinimas sumažino su fibroze susijusius biomarkerius. Šie atradimai rodo, kad terapinis antikūnas gali būti daug žadantis naujas gydymas pacientams, sergantiems įvairių tipų fibrozinėmis ligomis.
Būsimuose tyrimuose mokslininkai planuoja išbandyti gydymą kitomis fibrozinėmis ligomis, tokiomis kaip vilkligė ir hidradenitas suppurativa.
Tyrėjai nustato fibrozės kelią
Antrame neseniai atliktame tyrime mokslininkai siekė toliau suprasti mechanizmus, kurie skiria fibrozines ir nefibrozines odos ligas. Komanda palygino vienos ląstelės RNR sekos duomenis iš septynių skirtingų uždegiminių odos ligų.
Kai kurios ligos, pavyzdžiui, atopinis dermatitas ir psoriazė, buvo susijusios su paraudimu ir pleiskanojimu, bet ne su fibroze. Jie taip pat analizavo duomenis iš pacientų, sergančių fibrozinėmis ligomis, tokiomis kaip sklerodermija, transplantato prieš šeimininką liga ir vilkligė.
Jų analizė atskleidė, kad fibrozinės ligos buvo susijusios su didesniu baltymo, vadinamo STAT1, aktyvumu fibroblastuose, pagrindiniame ląstelių tipe, kuris yra hiperaktyvus sergant fibrozinėmis ligomis.
Norėdami geriau suprasti, kaip STAT1 sąveikauja su EGFR signalizacijos keliu, kad paskatintų fibrozę, mokslininkai sukūrė pelių modelius, kuriuose trūko STAT1. Kai komanda aktyvavo EGFR, jie nustatė, kad pelėms be STAT1 buvo mažiau fibrozės, palyginti su įprastais gyvūnų modeliais.
„Jei suaktyvinsime EGFR sukeldami sužalojimą, kai nėra STAT1, nė vienas fibrozinis genas nėra aktyvuojamas“, – sako Odell.
Tyrėjai atliko tolesnius eksperimentus su auginamais fibroblastais in vitro, kurie patvirtino, kad STAT1 reikalingas fibrozės atsiradimui.
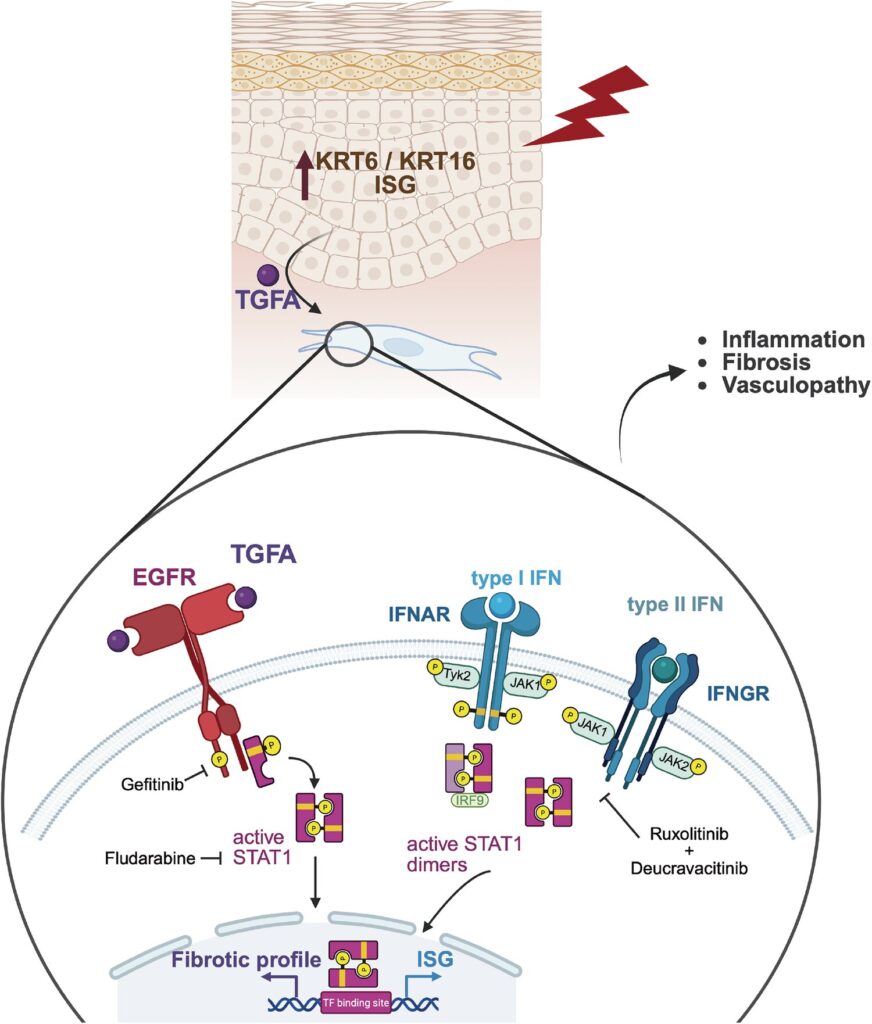
Šiuolaikiniai odos ligų gydymo būdai apima Janus kinazių (JAK) inhibitorius, kurie nukreipti į JAK-STAT kelią. Ankstesni tyrimai rodo, kad JAK aktyvinimas gali sukelti STAT baltymų, tokių kaip STAT1, aktyvumą. Nors JAK inhibitoriai gali sėkmingai gydyti odos ligas, tokias kaip atopinis dermatitas ir psoriazė, jie yra mažiau veiksmingi gydant fibrozę.
Dabartinis tyrimas rodo, kad EGFR signalizacija gali suaktyvinti STAT1 nepriklausomai nuo JAK, o tai gali paaiškinti, kodėl JAK inhibitoriai neveikia taip gerai sergant fibrozinėmis ligomis. Šis EGFR-STAT1 kelias yra perspektyvus naujas potencialių gydymo būdų tikslas, teigia mokslininkai.
Svarbu tai, kad EGFR-STAT1 kelio epiregulino aktyvacijos reguliavimas ne visada yra aktyvus – jis įjungiamas tik tam tikromis sąlygomis, pvz., Esant sužalojimui ar uždegimui.
„Tai nėra tikslai, kurių reikia norint gyventi kasdieniame gyvenime – nesitikime reikšmingo šalutinio poveikio juos slopindami“, – sako Odell. „Tikimės labai saugaus profilio.
Nauji tyrimai išryškina dvi perspektyvias terapines fibrozinių ligų gydymo galimybes. Mokslininkai tikisi, kad jie padės sukurti naujas priemones, kurios labai pagerins pacientų gyvenimo kokybę. „Yra daug vilčių dėl ateities“, – sako Flavell.