Keletas veiksnių daro kiaušidžių vėžį ypač sudėtingą gydyti. Taip yra daugiausia dėl to, kad vėžys dažnai plinta mikroskopiniu lygiu pilvoje anksti, todėl diagnozuojama pažengusia stadija. Be to, nors pradinis gydymas chirurgijos, chemoterapijos ir techninės priežiūros gydymo būdais daugeliui žmonių yra sėkmingi, labiausiai pažengę į kiaušidžių kiaušidžių vėžį galiausiai grįžta.
Dabar „Memorial Sloan Kettering“ vėžio centro (MSK) tyrimų komanda siekia rasti naujų būdų, kaip sustabdyti labiausiai paplitusią ir mirtiną kiaušidžių vėžio formą-aukšto lygio serozinį kiaušidžių vėžį-nuo pasikartojimo, naudojant metodą, kurį jie sukūrė siekiant sekti gydymo atsparumo ląstelių raidą kiaušidžių vėžyje.
Jų išvados, kurios yra paskelbtos Prigimtisgali padėti kurti naujus metodus, kaip nustatyti ir galiausiai nukreipti į specifinius ląstelių subpopuliacijas, sukeliančias pasikartojimą.
„Aukštos kokybės seroziniai kiaušidžių vėžys arba HGSOC yra įvairios ląstelių, iš kurių kai kurios bus jautrios mūsų geriausiems gydymams, o kai kurie-atsparūs“,-sako tyrimo pirmoji autorius Marc Williams, Ph.D., podoktorantūros tyrinėtojas, kuris naudoja skaičiavimo metodus vėžio evoliucijai tirti. „Tačiau esami šių vėžio atvejų stebėjimo būdai neišskiria vienos ir kitos gyventojų. Taigi, mes nusprendėme sukurti tokį, kuris galėtų.”
Kiaušidžių vėžio pokyčių stebėjimas laikui bėgant naudojant „Cloneseq-SV“
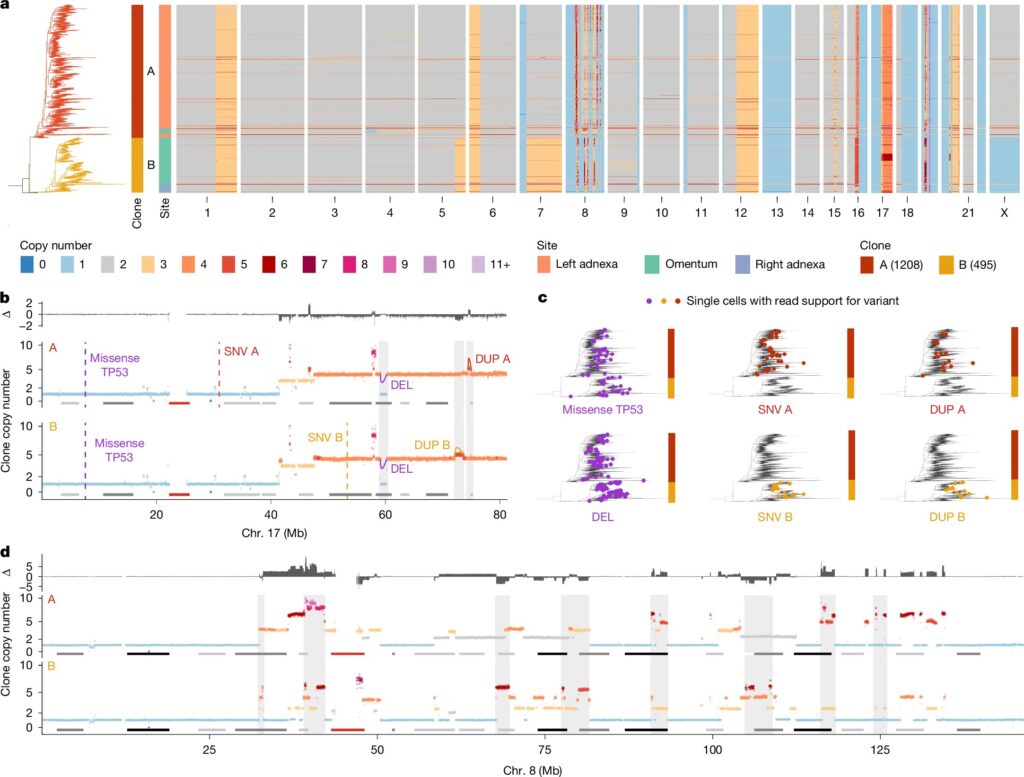
Norėdami pažvelgti į kiaušidžių vėžio ląstelių skirtumus ir kaip keičiasi jų sudėtis laikui bėgant, tyrimų komanda sukūrė metodą, kurį jie vadina Cloneseq-SV. Šis metodas sujungia vienos ląstelės viso genomo sekos nustatymą ir tikslinį struktūrinių variantų seką, tai yra didelio masto pokyčiai arba DNR pertvarkymai.
Tai leido mokslininkams stebėti vėžio evoliuciją, naudojant pradinius mėginius, paimtus operacijos metu, po to vykstančios kraujo tyrimų serijos, ir norint sekti, kurie naviko pogrupiai išgyvena gydymą ir kurie miršta.
„Iš esmės mes sugebėjome naudoti šiuos struktūrinius variantus kaip molekulinius„ juostų kodus “, kurie leido mums sekti navikinių ląstelių pogrupius kraujyje“, – sako vyresnysis tyrimo autorius Sohrabas Shahas, Ph.D., vadovaujantis MSK skaičiavimo onkologijos tarnybai ir tarnauja Halvorseno skaičiavimo onkologijos centro direktoriui.
Tyrime buvo analizuojami kraujo mėginiai, paimti iš 18 pacientų, sergančių HGSOC, nuo diagnozės nustatymo metu, pasikartojant jų vėžį.
„Naudodamiesi šiuo nauju metodu, galėjome pastebėti, kad diagnozės nustatymo metu buvo atsparios ląstelės ir kad jos galėjo daugintis kaip ląstelės, kurios buvo jautresnės gydymui, mirė“, – priduria dr. Shah.
Tyrimas nebūtų buvęs įmanomas be didelio skaičiavimo tyrėjų ir chirurgų, patologų ir onkologų, kurie specializuojasi ginekologinių vėžių srityse, bendradarbiavimo ir komandinio darbo MD ir ginekologijos ligos valdymo komandos tyrimų laboratorijos direktorius Britta Weigelt, Ph.D ..
Kaip „Cloneseq-SV“ galėtų padėti būsimiems pacientams
„Cloneseq-SV“ leido tyrėjams nustatyti aiškų modelį: vėžio ląstelių subpopuliacijos, kurios išryškėja pasikartojimo metu, turi skiriamuosius požymius, įskaitant tam tikrų vėžio varomų genų (onkogenų) amplifikaciją (onkogenus), chromotį (kai chromosoma sudužo į daugybę gabalų ir yra neskoningai susiuvami) ir ištisos genomo padvigubėjimo.
„Kartu šios išvados suteikia naujų galimybių kurti gydymo strategijas, skirtas pulti į pažeidžiamumus, susijusius su šiomis bruožais“, – sako dr. Williams.
Jis atkreipia dėmesį į tyrimo pavyzdį: Vienas pacientas turėjo išskirtinį atsaką į trastuzumabo deruxtecan (vaistą, kuris nukreiptas į onkogeną ERBB2) ir po metų liko be ligos. Analizė atskleidė, kodėl taip buvo-iš pradžių navike buvo ląstelių mišinys su ERBB2 amplifikavimu ir be jo, tačiau tada pirmosios eilės gydymas pašalino ląstelių populiaciją be amplifikacijos, galiausiai sukėlė vėžį su daugybe papildomų ERBB2 kopijų pasikartojimo metu.
„Ir kadangi mes turime vaistą, kuris konkrečiai nukreiptas į ERBB2, šis evoliucinis poslinkis paliko visą naviką, jautrų naujam, tiksliniam gydymui“, – sako dr. Shah.
Tolesni tyrimų žingsniai
Tolesni tyrimų žingsniai apima daugiau pacientų, siekiant nustatyti daugiau modelių, kurie galėtų vadovautis gydymo strategijomis, taip pat užfiksuoti turtingesnį naviko ląstelių įvairovės vaizdą, surenkant daugiau naviko mėginių stebėjimo procedūrų metu.
Be to, tas pats požiūris gali būti taikomas kitoms vėžio rūšims, kurioms taip pat būdingas didelis kintamumo lygis (genomo nestabilumas), pažymi tyrėjai.