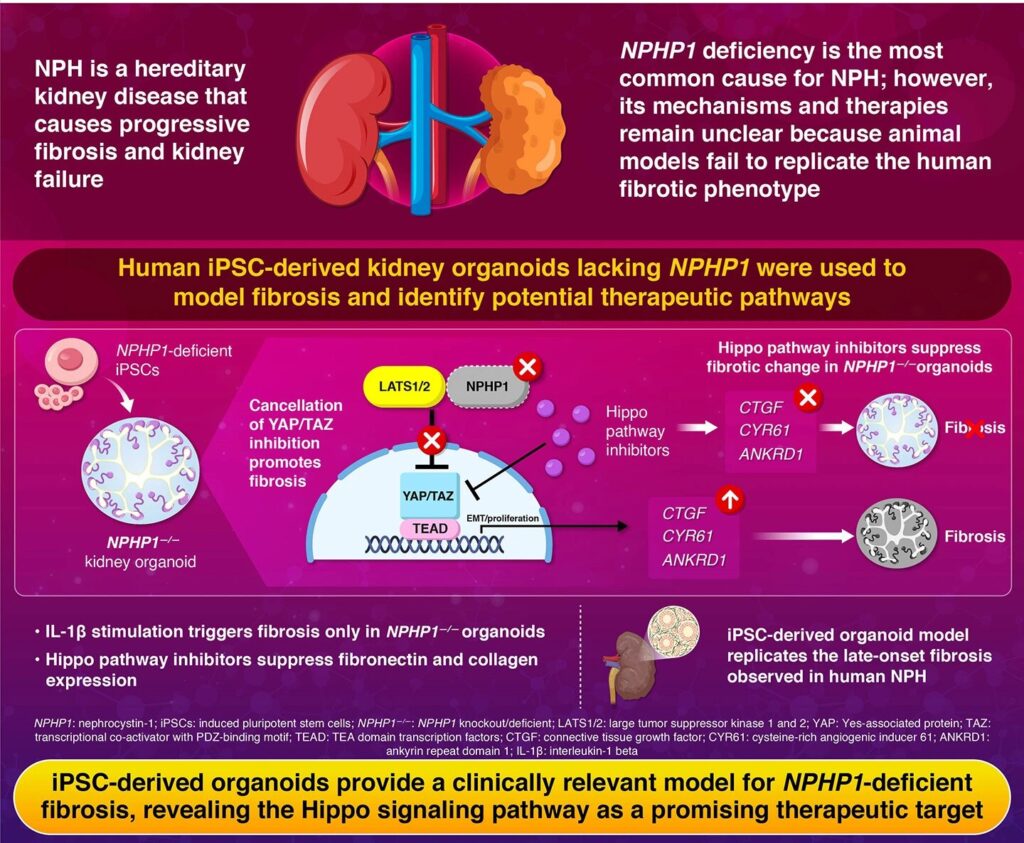
Naudodami žmogaus sukeltus pluripotentinius iš kamieninių ląstelių gautus inkstų organoidus, mokslininkai iš Science Tokyo atskleidė, kaip nenormalus Hippo signalizavimas skatina fibrozę sergant nefronoftize – genetiniu inkstų sutrikimu, kurį sukelia NPHP1 trūkumas.
Jų išvados paskelbtos m Kamieninių ląstelių tyrimai ir terapija, parodyti, kad Hippo signalizacijos kelio slopinimas veiksmingai slopina fibrozę inkstų audinyje. Tyrime pabrėžiamas organoidinių ligų modelių potencialas išaiškinti ligos mechanizmus ir pasiūlyti naują terapinį nefronoftizės tikslą.
Suprasti nefronoftizę ir jos iššūkius
Nefronoftizė (NPHP) yra paveldima inkstų liga, kuriai būdinga progresuojanti inkstų fibrozė, kuri apima nenormalų rando audinių kaupimąsi inkstuose. Tai viena iš pagrindinių vaikų ir jaunų suaugusiųjų galutinės stadijos inkstų ligos priežasčių, kuri sudaro apie 10 % visų vaikų dializės atvejų.
Nepaisant dešimtmečius trukusių tyrimų, iki šiol nėra jokio veiksmingo NPHP gydymo, išskyrus inkstų transplantaciją.
Liga dažniausiai atsiranda dėl mutacijų arba ištrynimų NPHP1 gene, kuriame pateikiamos instrukcijos, kaip gaminti nefrocistino-1 baltymą, būtiną sveikiems inkstų kanalėliams palaikyti. Tačiau tikslus ligos mechanizmas liko neaiškus, nes tinkami su NPHP1 susijusių NPHP gyvūnų modeliai nesugeba atkurti sunkių fibrozinių pokyčių, pastebėtų žmonėms.
Žmogaus inksto organoidinio modelio kūrimas
Siekdama įveikti šį ilgalaikį iššūkį, tyrėjų grupė, vadovaujama docento Eisei Sohara, jaunesniuoju docentu Koichiro Susa ir absolventu Takefumi Suzuki iš Nefrologijos katedros, Medicinos ir stomatologijos mokslų aukštosios mokyklos, Tokijo mokslų instituto (Tokijo mokslas), sukūrė žmogaus inksto organductoidinį modelį. (iPS) ląstelės.
„Siekdami modeliuoti NPHP1 trūkumą, pastebėtą sergant nefronoftize, naudojome genomo redagavimą, kad pašalintume NPHP1 geną“, – aiškina pagrindinis autorius Sohara. „Tokiu būdu mes sukūrėme NPHP1 trūkumų turinčias iPS ląstelių linijas, kurios vėliau išsiskyrė į trimačius inkstų organoidus.” Šios mini, savaime besitvarkančios inkstų struktūros gali tiksliai imituoti žmogaus nefrono architektūrą ir ląstelių sudėtį.
Kai šie NPHP1 trūkumo inkstų organoidai buvo veikiami žemo lygio uždegiminių signalų (interleukino-1β), jie parodė ryškius fibrozinius pokyčius, kurių nebuvo pastebėta normaliuose inkstų organoiduose.
Išsamios mikroskopinės ir molekulinės analizės atskleidė su fibroze susijusių genų, tokių kaip fibronektinas, kolagenas ir CTGF, per didelę ekspresiją, o tai rodo pagrindinio fibrozės signalizacijos kelio aktyvavimą NPHP1 trūkumo organoiduose.
Hippo signalizacijos kelio vaidmuo fibrozėje
Tolesnis tyrimas atskleidė nenormalų Hippo signalizacijos kelio aktyvavimą organoiduose, kuriuose trūksta NPHP1. Hippo signalizacijos kelias yra molekulinis tinklas, reguliuojantis audinių augimą ir atstatymą, padedantis išvengti per didelio randų susidarymo, kontroliuojant YAP ir TAZ baltymų – centrinių šio kelio aktyvatorių – aktyvumą. NPHP1 nebuvimas sutrikdo šį reguliavimą, todėl atsiranda nekontroliuojamas fibrozinis signalizavimas.
„Mūsų išvados rodo, kad NPHP1 sąveikauja su Hippo kelio komponentais, kad išlaikytų pusiausvyrą tarp atstatymo ir fibrozės”, – sako Sohara. „Kai ši sąveika prarandama, Hippo kelias tampa pernelyg aktyvus ir sukelia progresuojančią inkstų pažeidimą.”
Išbandomos terapijos ir ateities kryptys
Siekdama ištirti šio kelio blokavimo terapinį potencialą, komanda organoidiniame modelyje išbandė kelis Hippo kelio inhibitorius. Tarp jų taip pat buvo išbandytas verteporfinas – šviesa aktyvinamas vaistas, jau patvirtintas įprastai akių ligai, vadinamai geltonosios dėmės degeneracija, gydyti. Stebėtina, kad verteporfinas veiksmingai pakeitė fibrozės žymenis ir taip pat sumažino su fibroze susijusių genų kaupimąsi.
„Kadangi verteporfinas jau naudojamas klinikoje, jis siūlo greitą nefronoftizės gydymo galimybę”, – pažymi Susa.
Apskritai, šis tyrimas yra svarbus žingsnis link kamieninių ląstelių tyrimų pritaikymo praktiniams retų inkstų ligų gydymo metodams.
Kaip pirmasis tyrimas, skirtas sėkmingai išbandyti vaistus pagal žmogaus iPSC gautą NPHP modelį, jis parodo, kaip organoidinės technologijos gali pakeisti gyvūnų modelius, kad būtų galima tiksliau modeliuoti ligą ir atlikti individualizuotus vaistų tyrimus.
Ateityje mokslininkai planuoja patobulinti savo inkstų organoidinę platformą, kad galėtų ištirti papildomus signalizacijos būdus ir išbandyti daugiau vaistų, skirtų inkstų fibrozei, taip atveriant kelią saugesniam ir veiksmingesniam lėtinių inkstų ligų gydymui.