JK buvo atvejis, kai kuriama imunoterapija TGN1412 sukėlė citokinų audrą per kelias valandas po vartojimo žmonėms, o tai sukėlė daugelio organų nepakankamumą. Kitas pavyzdys, Aptiganel, kandidatas į vaistus nuo insulto, taip pat buvo labai veiksmingas gyvūnams, tačiau žmonėms jo vartojimas buvo nutrauktas dėl šalutinio poveikio, pavyzdžiui, haliucinacijų ir sedacijos. Ikiklinikinių tyrimų metu saugiais laikomi vaistai gali būti mirtini atliekant klinikinius tyrimus su žmonėmis.
Sukurta mašininiu mokymusi pagrįsta technologija, skirta išmokti šiuos skirtumus ir prevenciškai nustatyti potencialiai pavojingus vaistus prieš klinikinius tyrimus.
Tyrimų grupė, vadovaujama profesoriaus Sanguk Kimo iš Gyvybės mokslų katedros ir POSTECH Dirbtinio intelekto aukštosios mokyklos, kartu su Dr. Minhyuk Park ir Woominu Song iš Gyvybės mokslų katedros bei p. Hyunsoo Ahn iš Dirbtinio intelekto aukštosios mokyklos, sukūrė technologiją, kuri naudoja vaistų šalutinį poveikį žmonių mokymuisi.
Tyrimas paskelbtas internete m eBiomedicina.
Kuriant naujus vaistus, tie, kurie praeina ikiklinikinius tyrimus, dažnai rodo netikėtą toksiškumą žmonėms. Ši problema kyla dėl skirtingų žmonių ir gyvūnų biologinių reakcijų. Pavyzdžiui, šokoladas paprastai yra saugus žmonėms, bet toksiškas šunims. Panašiai, vaistas, kuris yra saugus pelėms, nebūtinai reiškia, kad jis yra saugus žmonėms.
Iki šiol šis „skirtumas tarp skirtingų rūšių“ buvo pagrindinė naujų vaistų kūrimo nesėkmių priežastis.
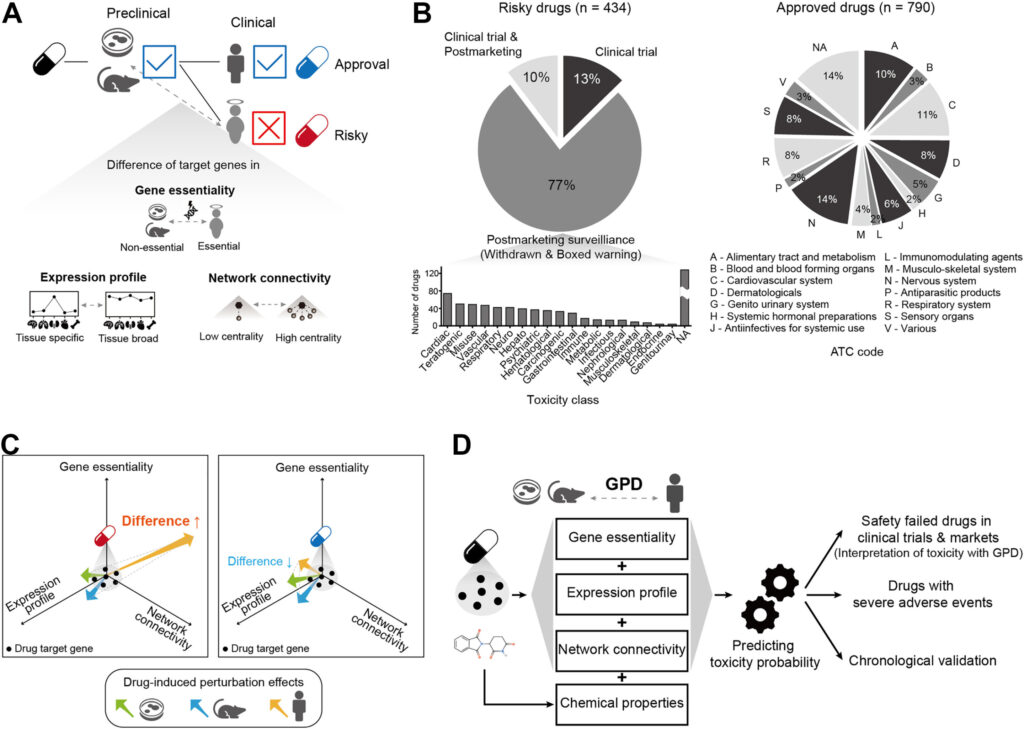
Tyrimo grupė daugiausia dėmesio skyrė „genotipo ir fenotipo skirtumui (GPD),” biologiniams ląstelių, pelių ir žmonių skirtumams. Jie analizavo, kaip genai, kuriems taikomi vaistai, veikia skirtingai žmonėms ir ikiklinikiniams modeliams, daugiausia dėmesio skirdami trims pagrindiniams veiksniams: pirma, geno trikdymo įtaka išgyvenimui (esmingumas); antra, genų ekspresijos įvairiuose audiniuose modelis; ir trečia, genų jungiamumas biologiniuose tinkluose.
Patvirtinimas naudojant 434 pavojingų vaistų ir 790 patvirtintų vaistų duomenis atskleidė, kad GPD charakteristikos buvo reikšmingai susijusios su vaistų nesėkme dėl toksiškumo žmonėms. Nuspėjamoji galia žymiai pagerėjo, nes buvo remiamasi vaistų cheminiais duomenimis, plotas po kreive (AUPRC1) padidėjo nuo 0,35 iki 0,63, o plotas po kreive (AUROC2) padidėjo nuo 0,50 iki 0,75.
Sukurtas AI modelis parodė puikų nuspėjamąjį našumą, palyginti su esamais moderniausiais modeliais.
Be to, jis parodė praktiškumą atliekant „chronologinį patvirtinimą“, kuris įspėja vartotojus apie vaistus, kuriuos dėl toksiškumo gresia pašalinimas iš rinkos. Iki 1991 m. parengus prognozavimo modelį tik vaistų duomenims, jis teisingai numatė vaistus, kurie, kaip tikimasi, bus pašalinti iš rinkos po 1991 m., pasiekęs 95 % tikslumą.
Šio tyrimo reikšmė yra ta, kad jis panaikina „vertimo atotrūkį“ tarp ikiklinikinių ir klinikinių tyrimų, kiekybiškai įvertindamas biologinius ląstelių, ikiklinikinių gyvūnų modelių ir žmonių skirtumus.
Farmacijos įmonės gali sumažinti kūrimo išlaidas ir laiką, prieš klinikinius tyrimus atrinkdamos didelės rizikos kandidatus, taip pat pagerindamos pacientų saugą. Tikimasi, kad modelio efektyvumas padidės, nes kaupiasi daugiau susijusių duomenų ir komentarų.
Profesorius Sanguk Kimas pareiškė: „Tai pirmasis bandymas įtraukti genotipo ir fenotipo santykių skirtumus, kad būtų galima prognozuoti vaistų toksiškumą. Mūsų sistema leidžia anksti nustatyti didelės rizikos vaistus klinikinėje plėtroje.”
Jis pridūrė: „Šis metodas žada sumažinti plėtros išlaidas, pagerinti pacientų saugą ir padidinti gydymo patvirtinimų sėkmės rodiklį.
Pirmieji autoriai dr. Min-hyuk Park ir p. Woomin Song teigė: „Į žmogų orientuotas toksiškumo prognozavimo modelis bus labai praktiška naujų vaistų kūrimo priemonė. Tikimės, kad farmacijos įmonės galės iš anksto atrinkti didelės rizikos vaistus ikiklinikinėje stadijoje, taip pagerindamos kūrimo efektyvumą.”